En una mañana de miércoles a finales de enero de 1896, en una pequeña fábrica de bombillas en Chicago, una mujer de mediana edad llamada Rose Lee se encontraba en el centro de un esfuerzo médico revolucionario. Con un tubo de rayos X posicionado sobre el tumor en su seno izquierdo, Lee fue tratada con una oleada de partículas de alta energía que penetraron en la masa maligna. Así, sin fanfarrias, nació la terapia con rayos X.
Desde esos comienzos, la radioterapia ha recorrido un largo camino. El descubrimiento del radio y otros metales radiactivos permitió administrar dosis más altas de radiación para atacar cánceres más profundos. La introducción de la terapia de protones permitió dirigir con precisión los haces de radiación a los tumores, reduciendo el daño a los tejidos sanos circundantes, una precisión que se perfeccionó aún más con los avances en física médica, tecnologías informáticas y técnicas de imagen de última generación.
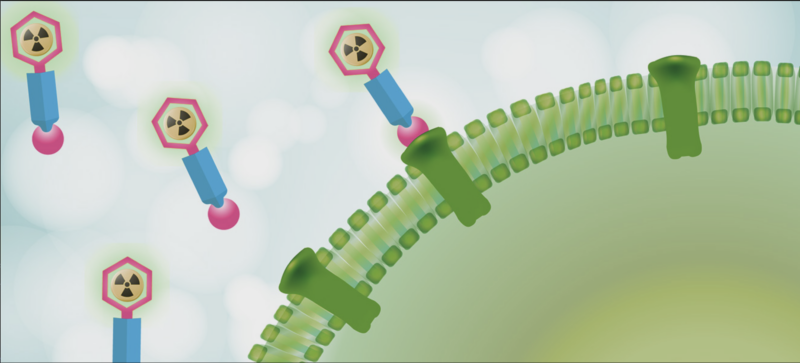
En el nuevo milenio, con la llegada de los radiofármacos dirigidos, el campo alcanzó un nuevo nivel de precisión molecular. Estos agentes, similares a misiles teledirigidos programados para cazar el cáncer, recorren el torrente sanguíneo para llevar sus cabezas nucleares radiactivas directamente al sitio del tumor. Hoy en día, solo un puñado de estas terapias están disponibles comercialmente para los pacientes, específicamente para formas de cáncer de próstata y tumores originados en células productoras de hormonas del páncreas y del tracto gastrointestinal. Sin embargo, este número está destinado a crecer a medida que los grandes actores de la industria biofarmacéutica comiencen a invertir fuertemente en la tecnología.
El 4 de junio, AstraZeneca completó la compra de Fusion Pharmaceuticals, fabricante de radiofármacos de próxima generación, en un acuerdo valorado en hasta 2.4 mil millones de dólares. Este movimiento sigue a transacciones similares realizadas en los últimos meses por Bristol Myers Squibb (BMS) y Eli Lilly, junto con adquisiciones anteriores de firmas innovadoras de radiofármacos por parte de Novartis.
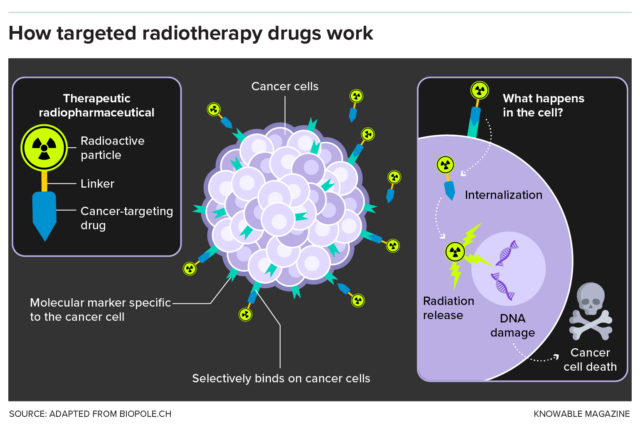
George Sgouros, físico radiológico de la Universidad Johns Hopkins, señala que este aumento de interés destaca un reconocimiento más amplio de que los radiofármacos ofrecen una manera fundamentalmente diferente de tratar el cáncer. No obstante, tratar el cáncer de manera diferente implica superar desafíos únicos, especialmente en la fabricación y distribución cuidadosamente programada de estas nuevas terapias antes de que la radiactividad decaiga. Expandir el alcance de la terapia para tratar una gama más amplia de cánceres también requerirá aprovechar nuevos tipos de partículas destructoras de tumores y encontrar objetivos adicionales adecuados.
Por décadas, una forma radiactiva de yodo fue el único radiofármaco disponible en el mercado, usado principalmente para tratar el cáncer de tiroides. Otros cánceres no tienen una afinidad comparable por elementos radiactivos, por lo que los investigadores tuvieron que diseñar medicamentos capaces de reconocer y adherirse a proteínas específicas producidas por las células tumorales. Los primeros agentes de este tipo en llegar al mercado estaban destinados estrictamente a obtener imágenes de los tejidos dentro del cuerpo. Esta innovación allanó el camino para los radiofármacos equipados con cargas radiactivas más potentes y letales, no solo para visualizar las células tumorales, sino para destruirlas.
La estrategia tardó en establecerse en el tratamiento rutinario del cáncer. El primer medicamento de este tipo aprobado en 1997, Quadramet, ofrecía alivio paliativo para el dolor óseo causado por el cáncer pero no estaba diseñado para reducir tumores. Los primeros años del 2000 vieron la llegada de dos nuevos medicamentos para el linfoma, ambos etiquetados con partículas radiactivas y dirigidos al marcador CD20 en las células sanguíneas malignas. Aunque funcionaron muy bien en ensayos clínicos, lucharon por ganar aceptación generalizada en la práctica clínica.
El interés por los radiofármacos disminuyó y la inversión en su desarrollo se estancó. Sin embargo, los esfuerzos en las universidades continuaron, como en Weill Cornell Medicine en Nueva York, donde Neil H. Bander inició ensayos con medicamentos de anticuerpos radiomarcados para tratar el cáncer de próstata en 2000. Estos medicamentos se diseñaron para unirse a un receptor de proteínas en la superficie de las células del cáncer de próstata, conocido como antígeno de membrana específico de próstata (PSMA).
Simultáneamente, en Europa, los clínicos desarrollaban agentes radiomarcados dirigidos a los receptores de somatostatina, presentes en raros cánceres del sistema neuroendocrino. Los investigadores descubrieron que las moléculas que imitan las hormonas cargadas con isótopos radiactivos se unirían a estos receptores y reducirían los tumores de manera efectiva. Una empresa francesa, Advanced Accelerator Applications (AAA), llevó uno de estos medicamentos marcados con lutecio a través de ensayos aleatorios, y en 2017, esta terapia demostró ralentizar significativamente la progresión de los tumores intestinales en comparación con el estándar de atención existente.
Eso llamó la atención de Novartis, que adquirió AAA por casi 4 mil millones de dólares. La adquisición de Endocyte por parte de Novartis trajo un agente dirigido a PSMA que demostró ser un verdadero cambio de juego para los pacientes con cáncer de próstata avanzado. En un ensayo clínico aleatorio, el medicamento, cuando se agregó a la atención estándar, más que duplicó el tiempo promedio antes de la progresión de la enfermedad y extendió la vida de los receptores por varios meses.
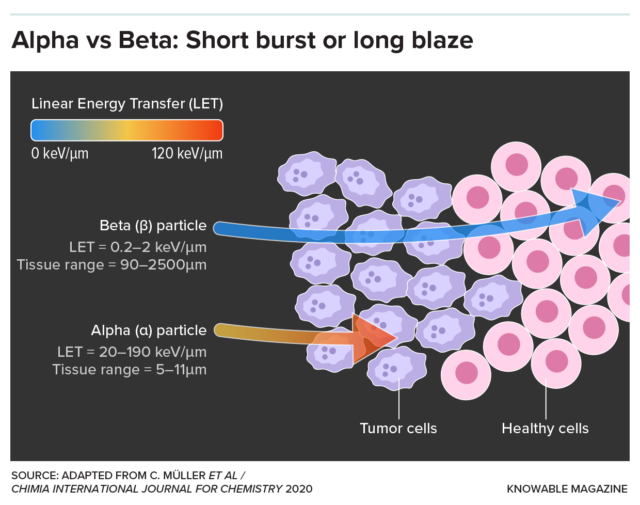
A medida que los investigadores desarrollan nuevas terapias que utilizan isótopos emisores de alfa, que son más grandes y energéticos que las partículas beta, esperan que estos agentes eventualmente eclipsen a Pluvicto. Los emisores de alfa permiten una destrucción celular altamente localizada mientras protegen las células sanas circundantes. A medida que las empresas buscan identificar nuevos objetivos para estos tratamientos, Novartis lidera la carrera con una nueva generación de medicamentos radiomarcados dirigidos a proteínas selectivas para el cáncer.
La fabricación de radiofármacos requiere una coordinación meticulosa entre clínicos y fabricantes para asegurar que los medicamentos lleguen a los hospitales en el momento adecuado. Novartis ha abierto una instalación de fabricación dedicada en Indianápolis, con la capacidad de producir cientos de dosis de Pluvicto diariamente, marcando un progreso significativo desde los días pioneros de Rose Lee en la fábrica de bombillas de Chicago.