La imagenología metabólica es una técnica no invasiva que permite a científicos y clínicos estudiar células vivas utilizando luz láser. Aunque es prometedora, enfrenta desafíos significativos, como la dispersión de la luz en los tejidos biológicos, lo que limita la profundidad de penetración y la resolución de las imágenes obtenidas. Sin embargo, un equipo de investigadores del MIT ha desarrollado un método innovador que supera estas limitaciones, duplicando la profundidad alcanzable y mejorando la velocidad y calidad de las imágenes.
Este nuevo enfoque no requiere cortar, procesar o teñir los tejidos previamente, algo común en técnicas tradicionales para crear contraste en imágenes. En lugar de ello, utiliza un láser especializado que ilumina las moléculas intrínsecas de las células, provocando la emisión de luz. Esto permite una representación más natural y precisa de la estructura y función de los tejidos.
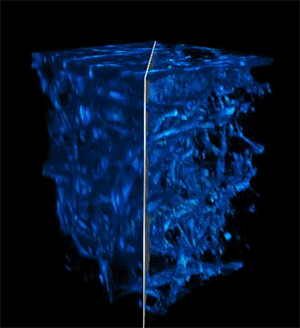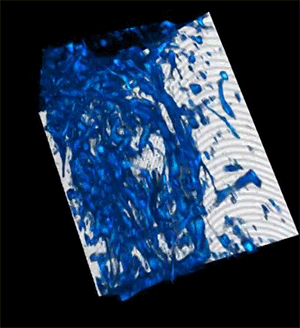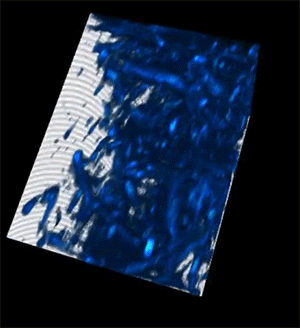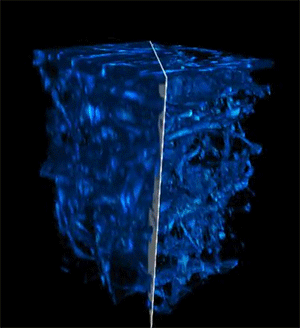
El avance clave fue personalizar la luz láser para penetrar en tejidos profundos. Gracias a un dispositivo innovador llamado «fiber shaper», los investigadores ajustaron el color y los pulsos de la luz para minimizar la dispersión y maximizar la señal al atravesar el tejido. Este control adaptativo permite generar imágenes más claras y detalladas, incluso en tejidos vivos.
Destaca por tres características principales:
- Mayor profundidad de penetración: logra superar los 700 micrómetros en muestras biológicas, en comparación con los 200 micrómetros alcanzados por técnicas previas.
- Velocidad mejorada: permite recopilar datos más rápidamente, capturando dinámicas metabólicas en tiempo real.
- Resolución superior: posibilita estudiar estructuras celulares con un nivel de detalle sin precedentes.
Estas ventajas lo convierten en una herramienta ideal para aplicaciones exigentes como la investigación del cáncer, la ingeniería de tejidos, el descubrimiento de fármacos y el estudio de respuestas inmunológicas.
La capacidad de penetrar profundamente y captar imágenes en vivo abre nuevas oportunidades en varias áreas biomédicas:
- Estudio de organoides: Los organoides, que imitan la estructura y función de órganos, son fundamentales para investigar enfermedades y evaluar tratamientos. Este método permite observar sus desarrollos internos sin dañarlos, facilitando el monitoreo continuo de sus estados metabólicos.
- Investigación en dinámica celular: La velocidad y profundidad de las imágenes permiten analizar cómo el metabolismo celular influye en la dirección y rapidez del movimiento celular, información crucial en áreas como la inmunología y la oncología.
- Avances en imágenes en 3D: Los investigadores están trabajando en algoritmos para reconstruir estructuras tridimensionales completas con alta resolución, abriendo nuevas posibilidades para la visualización y comprensión de sistemas biológicos complejos.
Los investigadores también planean aplicar esta técnica en el mundo real para evaluar en tiempo real cómo los medicamentos afectan el metabolismo celular. Esta capacidad podría acelerar el desarrollo de nuevos tratamientos y mejorar el diagnóstico de enfermedades complejas, como el cáncer.
El proyecto, liderado por Sixian You y Kunzan Liu, ha involucrado a expertos de múltiples disciplinas del MIT. La técnica se enmarca dentro de la categoría de imágenes sin etiquetas (label-free imaging), donde los láseres generan fluorescencia en moléculas específicas, eliminando la necesidad de tinción que podría dañar los tejidos.
Con miras al futuro, los investigadores están desarrollando fuentes de láser con bajo nivel de ruido para profundizar aún más en los tejidos con una menor dosis de luz. También buscan colaborar con biólogos, ingenieros y clínicos para trasladar este avance a aplicaciones médicas reales.
El impacto de esta tecnología no se limita al MIT. Melissa Skala, investigadora del Instituto Morgridge, señala que estas herramientas de imagenología metabólica permitirán explorar dinámicas metabólicas únicas, especialmente en sistemas vivos dinámicos, como las células inmunitarias en vasos sanguíneos. Por su parte, Irene Georgakoudi, profesora de ingeniería biomédica en la Universidad de Tufts, resalta que las capacidades de esta técnica —profundidad, velocidad y resolución— ampliarán significativamente las posibilidades en el diagnóstico de cáncer y la investigación en neurociencia.