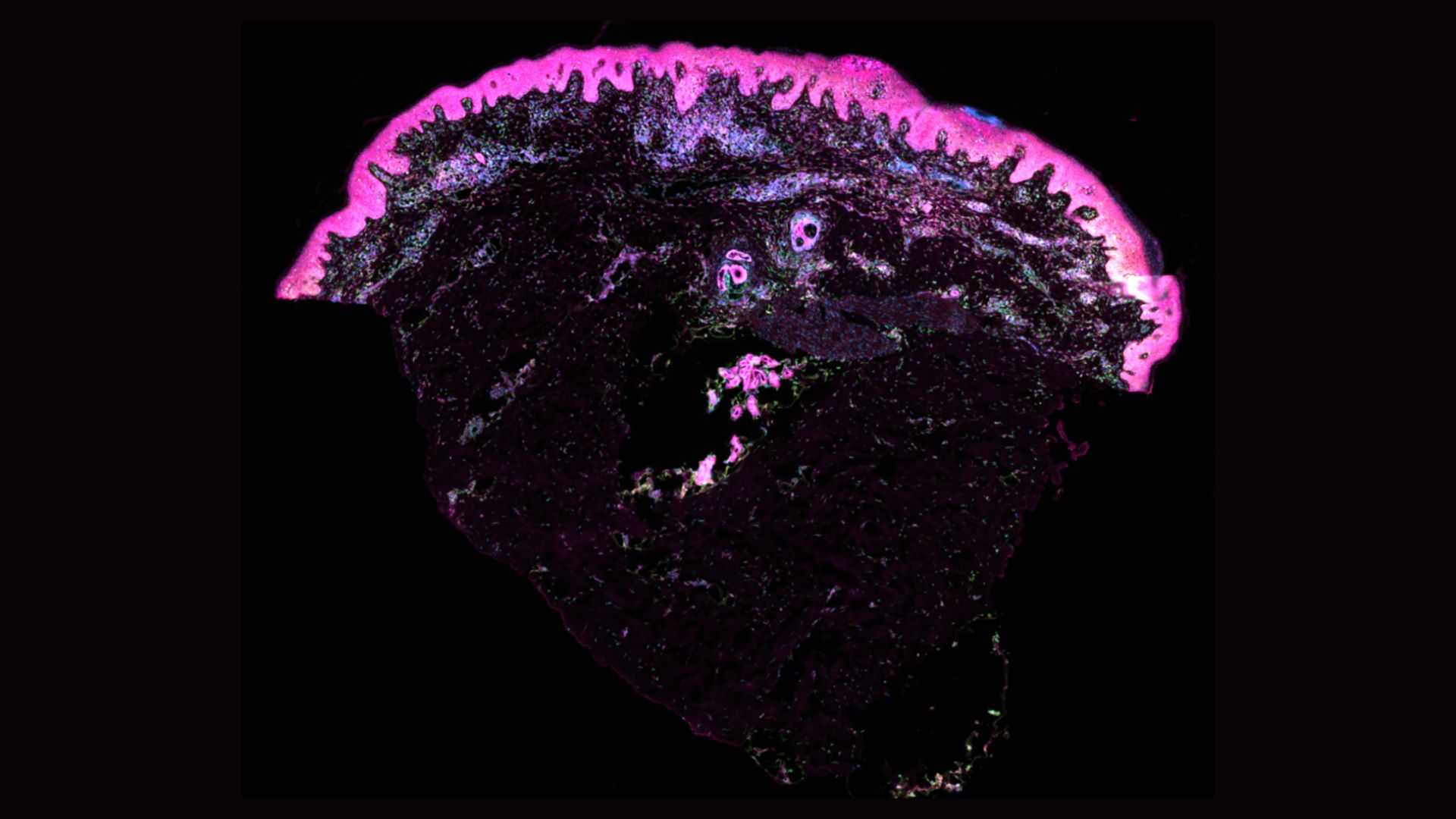
Un equipo de científicos del Instituto Wellcome Sanger y la Universidad de Newcastle ha logrado por primera vez trazar el desarrollo prenatal de la piel humana, proporcionando una visión sin precedentes de su morfología. Este trabajo ha permitido crear un detallado atlas de células individuales de la piel antes del nacimiento, ofreciendo nuevos conocimientos sobre cómo se forman los folículos pilosos y qué fallos pueden causar ciertas enfermedades cutáneas.
La investigación, liderada por la profesora Muzlifah Haniffa, ha dado lugar a herramientas que estarán disponibles para la comunidad científica, permitiendo estudiar enfermedades congénitas de la piel y explorar nuevas vías en la medicina regenerativa. Este avance promete mejorar tratamientos en áreas como los injertos de piel y la restauración capilar, gracias a los nuevos conocimientos sobre la formación y regeneración de la piel.
Para llevar a cabo este atlas, se utilizaron técnicas genómicas avanzadas como la secuenciación de células individuales y la transcriptómica espacial. Estas tecnologías han permitido examinar a nivel molecular el desarrollo de la piel, brindando una visión detallada de los procesos genéticos y celulares implicados. La creación de este mapa de la piel prenatal tiene implicaciones significativas para la investigación de trastornos cutáneos congénitos, como los que causan ampollas o piel escamosa, y podría abrir nuevas puertas en el desarrollo de tratamientos para estas afecciones.
Un aspecto clave de esta investigación ha sido la creación de una versión miniaturizada funcional de la piel humana en el laboratorio, conocida como organoide. Este organoide, además de replicar características de la piel, tiene la capacidad de producir pelo, lo que permitió a los científicos estudiar el papel de las células inmunitarias, como los macrófagos, en la formación de vasos sanguíneos y la cicatrización sin dejar cicatrices, un proceso que ocurre de forma natural en la piel prenatal.
El descubrimiento del papel crucial de los macrófagos en la vascularización y la cicatrización sin cicatrices podría tener un impacto significativo en el tratamiento de heridas y la recuperación postoperatoria. Al centrarse en la piel prenatal, que se desarrolla en un entorno estéril y tiene una capacidad regenerativa única, los investigadores han proporcionado un marco ideal para comprender las etapas iniciales del crecimiento de la piel.
Uno de los avances más emocionantes de este estudio es su aplicación potencial en la medicina regenerativa. Los resultados ofrecen una “receta molecular” para crear piel, lo que podría beneficiar a personas que necesitan trasplantes de piel, como víctimas de quemaduras o pacientes con alopecia cicatricial. Además, al entender mejor cómo se forman los folículos pilosos antes del nacimiento, los científicos confían en poder replicar este proceso, brindando esperanza a quienes han perdido el cabello por enfermedades o lesiones.
El uso de células madre adultas para desarrollar estos organoides ha sido otro aspecto crítico del estudio. Los organoides creados se asemejan más a la piel prenatal que a la piel adulta, lo que los convierte en un modelo ideal para investigar enfermedades cutáneas congénitas. Además, el descubrimiento de que algunos marcadores genéticos vinculados a trastornos de la piel ya están presentes antes del nacimiento sugiere que estas afecciones tienen su origen en las primeras etapas del desarrollo, lo que podría facilitar el desarrollo de terapias más específicas.
La doctora Hudaa Gopee, coautora del estudio, destacó la importancia del modelo de organoide para el crecimiento de cabello y el papel de los macrófagos en la formación de vasos sanguíneos y la reparación de la piel sin cicatrices. Estos hallazgos podrían ayudar a mejorar otros modelos organoides y avanzar en el campo de la medicina regenerativa, especialmente en la cicatrización sin cicatrices tras una cirugía.